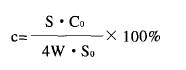| 膜技术分离纯化绿原酸提取液的研究 |
| 发布时间:2011-01-21 信息来源:admin 发布人:admin 点击次数:4745 |
吴正奇 ,凌秀菊 ,石勇 ,陈道玉z,李先芝z (1.湖北 [业大学生物工程学院,湖北武汉430068;2.湖北劲牌公司技术中心,湖北大冶435100) 摘 要:本实验研究了膜技术分离纯化绿原酸提取液的过程。先, 以透水通量为指标, 比较了两种微滤膜MF1和MF2、两种超滤膜UF1和UF2及两种纳滤膜NF1和NF2对绿原酸提取液的过滤特性。结果表明,MF2膜的通量可高达167.7kg/h,UF2膜的通量可达148.8kg/h和NF2膜的通量可达109.8kg/h,分别明显高于MF1(103.6kg/h)、UFl(48.0kg/h)~H NFl(45.6kg/h);其次,研究了浓缩液的水洗对绿原酸截留率的影响。结果表明,经一次水洗后,MF2膜的截留率可由12.5%降低到3.4%,UF2膜的截留率可由15% 降低到8%;最后,分析了膜分离过程中各物料的成分。结果表明,纳滤浓缩液含绿原酸为17964mg/L, 比原提取液提高了24.8倍,绿原酸的纯度由2.8%上升到27%。 关键词:金银花;绿原酸;膜技术; 纳滤 金银花含有芳香油、绿原酸、黄酮、皂苷和鞣质等生物活性成分,是重要的药食两用植物原料,在食品工业和医药工业中应用广泛[1,2] 。在食品工、 中,主要是利用水蒸汽蒸馏法提取金银花中的芳香油用于金银花露饮料的生产[3],而金银花蒸馏残渣直接被废弃,蒸馏残渣中含量较高的、具有重要药理作用的绿原酸等生物成分并没有加以回收利用,资源浪费严重,而且污染环境。绿原酸具有清除体内自由基和抗氧化作用、抑制突变和抗肿瘤、保护心血管、保肝利胆作用、抗菌、抗病毒等作用[4,5],广泛应用于食品工业、医药工业和日用化妆品工业中,价格昂贵。提取和纯化绿原酸方法有水提醇沉法、水提石灰乳沉淀法、醇提铅盐沉淀法、超声波法、聚酰胺柱层析法、酶法、超临界法和大孔树脂吸附法等。这些方法存在提取率低、对绿原酸的破坏大、处理量小、工艺过程长、产品纯度不高、卫生安全性差和成本高的缺点l5_101。在深入分析金银花蒸馏残渣的成分种类、结构、理化性质和膜技术[ 11的特点的基础上,我们提出用微孔过滤分离固体微粒、用超滤除去大分子物质、用纳滤浓缩的膜技术工艺处理绿原酸提取液以达到分离纯化和浓缩金银花蒸馏残渣的绿原酸提取液的目的,为后续制备高纯度绿原酸创造条件。 1 材料与方法 1.1 材料 1.1.1 原料 金银花蒸馏残渣 湖北劲牌有限公司。 1.1.2 试剂 盐酸(分析纯) 滨海煌舟化工有限公司;氯氧化钠(分析纯) 滨海煌舟化工有限公司; 甲醇、磷酸、乙腈、MERCK(高纯液相色谱纯溶剂) 德国MERCK公司。 1.1.3 仪器与设备 AB104.N型电子天平梅特勒.托利多仪器(上海)有限公司;电热蒸馏水器 上海华南医疗器械厂;H-H.2数显电热恒温水浴锅 金坛市富华仪器有限公司;320.3PHpH计梅特勒.托利多仪器(上海)有限公司;DOSJ.308A电导率仪 上海雷磁仪器厂;TD.5A台式离心机 湖南凯达科学仪器有限公司;Tu.1901双紫外可见光光度计北京普析通用仪器有限公司;Agilent 11o0高效液相色谱仪 美国安捷伦公司;C Prostar 230泵、Prostar 330二级陈列检测器 美国瓦里安公司;MN.103袋式过滤器上海迅纳科技有限公司;试验型组合膜分离设备(含多种膜组件) 湖北工业大学膜技术研究所;DZK.103恒温真空干燥箱上海迈捷仪器仪表有限公司。 1.2 方法 1.2.1 工艺流程
1.2.2 绿原酸提取液的制备 在水蒸汽蒸馏提取芳香油的过程中(约4h),金银花的组织结构已完全软化和破坏,故可以直接用水在室温下从金银花提油残渣中提取绿原酸。金银花提油残渣与水以1:1的比例混合打浆,用15% NaOH和HC1在不断搅拌的条件下调节混合浆液的pH6.5~7,用袋式过滤器过滤,挤压滤渣。滤渣再加1:1的水打浆,调节PH6.5~7, 过滤,挤压滤渣,合并滤液,即得绿原酸提取液。 1.2.3 绿原酸提取液的微孔过滤 分别选用MF1和MF2膜对绿原酸提取液进行微孔过滤,以除去不溶性固体微粒。在微孔过滤实验中,分别称取MF1和MF2膜的透过液和原始液质量,并记录各自的微孔过滤时间, 计算透水通量和浓缩倍数,根据透水通量的大小选择适当的微孔过滤膜。 1.2.4 微孔透过液的超滤 经微孔过滤处理后的绿原酸透过液,分别选用UF1和UF2膜对其进行超滤,以除去大分子物质及胶体物质,如蛋白质、多糖(淀粉、纤维素等)、鞣质或其复合物等。在超滤实验中,分别称取UF1和UF2膜的透过液和原始液质量,并记录各自的超滤时问,计算透水通量和浓缩倍数,根据透水通量的大小选择适当的超过滤膜。 1.2.5 超滤透过液的纳滤实验 经超滤处理后的绿原酸透过液,分别选用NF 1和NF2膜对其进行纳滤处理,以除去水(浓缩)及小分子物质(脱盐),如无机盐等。在纳滤实验中,分别称取NF1和NF2膜的透过液和原始液质量,并记录各自的纳滤时问, 计算透水通量和浓缩倍数,根据透水通量的大小和绿原酸的截留率选择适当的纳滤膜。 1.2.6 水洗对绿原酸的截留率的影响 分别取MF2微滤和UF1及UF2超滤的浓缩液,各加等质量的去离子水,搅拌,再分别用MF2、UF1和UF2膜对其进行微滤和超滤,至原浓缩液质量,分别测定微滤和超滤浓缩液以及微滤和超滤透过液中绿原酸的含量,分别计算水洗前后绿原酸的截留率。 1.2.7 膜分离过程各物料的成分分析 分别取MF2.UF2.NF2膜分离过程的各物料样品,测定其绿原酸的含量、电导率和总可溶性固形物的含量。 1.3 测定与分析方法 1.3.1 透水通量与截留率测定[11] 在膜分离过程中,分另0称取相应的原始液和透过液质量,并记录各自的膜分离时间。分别测定相应的原始液、透过液和浓缩液中的绿原酸的含量,按下述公式分别计算相应的透水通量、浓缩倍数和绿原酸的截留率:
式中,v为透水通量(kg/h);n为浓缩倍数;c为绿原酸的截流率(%);w 为透过液的质量(kg);T为膜分离时间(h);Wo为起始液的质量(kg);W 为膜分离的浓缩液或水洗后浓缩液的质量(kg);C 为膜分离的浓缩液或水洗后浓缩液巾绿原酸的浓度(mg/L);W 为绿原酸粗提取液经袋式过滤器过滤后液体的质量(kg);C为绿原酸粗提取液经袋式过滤器过滤后液体的绿原酸浓度(mg/L)。 1.3.2 HPLC法测定绿原酸含量[12] 1.3.2.1 色谱分析条件 Agilent l 100型HPLC仪,ZORBAX XDB―CI8柱(ID4.6×150mm,5 m,pn为993967―902,sn为USKH012889);柱温:30℃ ;流动相: 乙腈/0.4磷酸水=11/89;流速:0.8ml/min;检测波长:327nm,Prostar410型自动进样器。 1.3.2-2 对照品溶液的制备 精密称取绿原酸对照品5.1mg,用30% 甲醇超声溶解定容至10ml,再精密吸取2ml于10ml容量瓶中,用30% 甲醇稀释定容至10ml,作为对照品溶液备用。 1.3.2-3 供试品溶液的制备 精密量取样品溶液lml于lOml容量瓶中,用30% 甲醇稀释至刻度,摇匀,用0.45 m微孔滤膜过滤,作为供试品溶液备用(视样品含量不同取样量略有不同――保证供试品溶液中绿原酸的含量在100mg/L左右1。 1.3.2-4 绿原酸含量计算 对照品溶液以及供试品溶液各进样10 l,记录结果,根据保留时间进行定性,相对应色谱峰的峰面积进行定量,计算相应绿原酸含量。公式[18]如下:
式中,s为样品峰面积;s o为对照品峰面积;c。为对照浓度(mg/L);W 为样品重量(mg);1/4为为测定常数。 1.3.3 电导率的测定[13] 用电导率仪分别测定膜分离过程中各物料的电导率, 以电导率表示相应物料中的盐类物质的相对含量。 1.3.4 总可溶性固形物含量的测定[13] 将膜分离过程中的物料各精确取样,放入干燥箱中, 于105℃干燥至恒重,测定相应的总可溶性固形物的含量。 2 结果与分析 2.1 微滤膜的选择 由于金银花在水蒸汽蒸馏过程中长时间受热,其组织结构已完全解体,蒸馏残渣的绿原酸提取液中含有大量的固体微粒,根本无法过滤。微孔过滤是除去不溶性固体微粒的有效方法, 但微滤膜材料不同,微孔过滤的透水通量可能会有很大的不同。微滤膜MF1和MF2的平均透水通量见表1(40℃,P=0.1MPa)。由表1可知,MF1膜在7.7倍浓缩时的平均透水通量是103.6kg/h,而MF2膜在1 1、8倍浓缩时的平均透水通量是176.7kg/h,MF2膜的平均透水通量远大于MF1膜,这可能是因为提取液中的某些成分容易堵塞MFI膜的膜孔或MF1膜材料容易导致浓差级化,从而降低了透水通量。故微滤实验过程选用膜MF2。
2.2 超滤膜的选择 金银花在水蒸汽蒸馏过程中长时间受热, 其组织结构已完全解体,金银花中的大分子物质及胶体物质完全进入绿原酸提取液中,蒸馏残渣的绿原酸提取液十分浑浊,根本无法澄清。超过滤是除去提取液中的大分子物质及胶体物质,如蛋白质、多糖(淀粉、纤维素等)及其复合物等,使溶液澄清化的良好方法。超滤膜材料不同, 超滤的透水通量和过程的有效性可能有差异,超滤膜UF1和UF2平均透水通量见表2(45~50℃ ,P=0.3MPa1。由表2可知,UF1膜在13.2倍浓缩时的平均透水通量是48.0kg/h,UF2膜在16.7倍浓缩时的平均透水通量是148.8kg/h,UF2膜的平均透水通量远大于UF1膜,可能是由于一些蛋白质、多糖类大分子物质更容易堵塞超滤膜UF1的膜孔,使透水通量降低。故超滤实验选用膜UF2为宜。
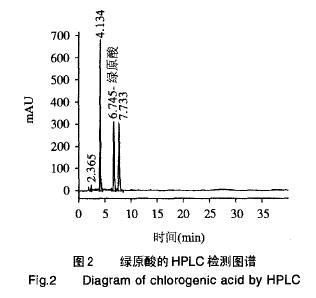
2.3 纳滤膜的选择 纳滤可以除去提取液中的水分及少量小分子物质,如无机盐等, 达到浓缩和部分脱盐的目的。纳滤膜的种类、结构与膜孔大小不同对纳滤过程的透水通量和绿原酸的截留率(透过液中绿原酸的浓度)会产生不同的影响。纳滤膜NF1和NF2的平均透水通量和透过液中绿原酸的浓度见表3(45-50℃,P=1.1MPa)。由表3可知,NF1在18.9倍浓缩时的平均透水通量是45.6kg/h,透过液中绿原酸的浓度为90.9mg/L(绿原酸的HPLC检测图谱见图2);NF2在20.0倍浓缩时的平均透水通量是109.8kg/h,透过液中绿原酸的浓度为3.33mg/L。NF2膜的平均透水通量远大于NF1膜,而透过液中绿原酸的浓度远低于NF1膜,这可能是因为NF2膜是一种带负电荷的离子膜,在纳滤过程中能排斥带负电荷的绿原酸等小分子物质(纳滤过程中物料的pH为6.5~7),从而使绿原酸、鞣质等带负电荷的小分子物质不易堵塞膜孔,不易在膜表面沉积, 也不易进入膜孔造成膜堵塞和膜污染的缘故。所以纳滤过程应该选用膜NF2。
2.4 水洗对绿原酸截留率的影响 膜分离过程会产生浓缩液,当浓缩液的体积小到不足以形成回流时,膜分离过程就不能进行。但是浓缩液中还含有比较高浓度的绿原酸,为了充分回收绿原酸,采用浓缩液加水稀释以形成膜回流的水洗工艺是必要的。加与浓缩液等质量水的水洗前后,MF2、UF1和UF2膜的绿原酸截留率见表4。由表4中数据可知,微滤、超滤的浓缩液经过等质量水洗后,膜对绿原酸的截留率均明显降低了,尤其是微滤膜MF2的浓缩液经一次等质量水洗后绿原酸的截留率大幅度地降低。
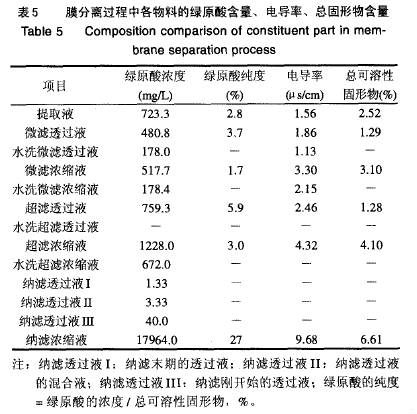
2.5 适宜的膜过滤工艺 上述一系列实验结果表明,选用MF2 UF2 NF2的膜组合过滤,无论是透水通量还是绿原酸的截留率,均要明显优于MF1.UF1.NF1的膜组合。MF2.UF2.NF2的膜组合过滤,绿原酸的总截留率为12.4%(EP绿原酸的总回收率为87.6%)。所以绿原酸提取液的分离纯化应该选用MF2一UF2一NF2的膜组合。 2.6 膜分离过程各物料的成份分析结果 在膜过滤过程中,各物料的绿原酸(绿原酸的HPLC图谱见图2)含量、电导率、总固形物含量的测定结果见表5。由表5可知,经MF2.UF2.NF2组合的膜分离过程,绿原酸的浓度由723.3mg/L浓缩至17964.0mg/L,浓度提高了24.8倍;绿原酸的纯度由2.8%上升到27%,纯度提高了9.6倍;而总可溶性固形物由2.52%增加到6.61%,提高了不到3倍,这说明MF2.UF2.NF2组合的膜分离过程对绿原酸提取液的纯化和浓缩效果十分显著。同时,提取液的电导率也由1.56ta s/cm上升至9.68ta s/cm,增大到了6.2倍,说明提取液中的无机盐等带电物质等并未除去多少,纳滤浓缩液的灰份很大。由于MF2.UF2.NF2组合的膜分离过程除去了固体微粒和大分子物质,纳滤浓缩液的固形物主要是绿原酸、黄酮、鞣质、皂苷、二糖、三糖和无机盐等小分子物质。 3 结论 由于膜分离技术具有低温无相变和对大、小分子物质的分离效果好等特点,故特别适合于热敏性的绿原酸提取液的分离纯化与浓缩。纳滤浓缩液中的绿原酸含量虽然很高,但是其
中存在大量的与绿原酸结构相似、分子量相近、性质近似的黄酮、鞣质、皂苷、糖类物质,如何从纳滤浓缩液中分离绿原酸,得到高纯度的绿原酸,将是下一步的研究内容。 参考文献: [1]吴立军.中药化学[M].北京:中国医药科技出版社,2001.189 225. [2] 董克满.金银花的化学成分及生物活性⋯.齐齐哈尔医学院学报,2003(6):692―694. [3] 何文裴,李士敏.正交试验探讨金银花挥发油的提取条件『J1.中国中药杂志.2003(2):172.173. [4] 高锦明,张鞍灵,张康健,等.绿愿酸的分布、提取与生物活性综述fJ].西北林学院学报,1999(2):73.82. [5]刘军海,裘爱泳.绿原酸及其提取纯化和应用前景【J】.粮食与油脂,2003(9):44―46. [6]赵钟兴,韦藤幼,郝瑞然。等.金银花中提取绿原酸生产工艺的改进[J].时珍国医国药,2004(12):829 830. [7]金许东颖。盛家荣,覃永周.银花中绿原酸提取方法的比较和优化研究【J】广西师范学院学报:自然科学版,2003(2):17 20. [8]尉圻,马希汉.绿原酸及其提取分离方法评述⋯.中成药,2001(2):135 138. [9]林丹,赵国玲,刘佳佳.金银花不同提取方法的绿原酸比较研究[J].天然产物研究与开发,2003(2):124 126. [10]刘佳佳,赵国玲,章晓班,等.金银花绿原酸酶法提取新:岂研究【J】.中成药。2002(6):416.418. [11]郑领英,王学松.膜分离技术[M].北京:化学工业出版社,2000:30145. [11]许贵军,隋金婷.HPLC法确定金银花最佳采收时期【J】.黑龙江医学,2002(I 1):866 870. [12]大连轻工业学院.食品分析[M].北京:中国轻Z.Ak出版社,1994:779n. 产品链接: 杜仲提取物 绿原酸 金银花提取物 苦杏仁苷 枇杷叶提取物-熊果酸 大花紫薇提取物-科罗索酸 上禾生物 专注植提 精于高纯 基于您对天然产物需求持续创新 |







 膜技术分离纯化绿原酸提取液的研究
膜技术分离纯化绿原酸提取液的研究