| 水提醇沉法从葵花籽中提取绿原酸 |
| 发布时间:2010-12-17 信息来源:admin 发布人:admin 点击次数:3754 |
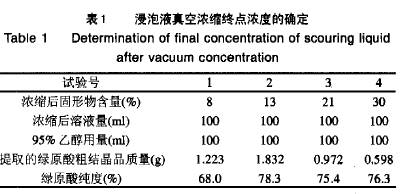
郑喜群1,2,蒋继丰1,刘晓兰1,孙秀云1 (1.齐齐哈尔大学生命科学与工程学院,黑龙江齐齐哈尔 161006: 2.中国农业大学食品科学与营养工程学院,北京 100083) 摘 要:绿原酸具有抗菌、抗病毒、抗氧化等生物活性。葵花籽富含绿原酸。以水酶法提取葵花籽油脂后分离出的水浸提液为原料,采用醇沉淀法去除浸提液中的多糖,抽滤浓缩滤液后得到绿原酸。多次实验结果表明,浸提液浓缩到固形物含量在13% 时,加入浸提浓缩液体积l倍量的95% 的乙醇沉淀并过滤掉多糖,反复处理两次,滤液再经真空浓缩得到纯度76% 左右的绿原酸。 关键词:葵花籽;浸提液:绿原酸; 多糖 绿原酸(chlorogenic acid)又名咖啡酸,是植物在有氧呼吸过程中产生的一种物质,分子式C H-sO,,分子量345.30。绿原酸主要存在于杜仲、金银花,葵花籽中,是半水状化合物或微黄色针状晶体,25℃时在水中溶解度为4%,热水中溶解度更大,并且随温度降低溶解度逐渐降低[1]。绿原酸易溶于乙醇、丙酮,微溶于乙酸乙酯,难溶于氯仿、乙醚等极性有机溶剂[2]。毒性很小,幼大鼠口服LD s0大于1g/G。绿原酸具有广泛的生物活性,对急性咽喉炎症的化脓,皮肤病有显著疗效, 具有抗菌、抗病毒、止血、增高白血球[3],缩短血凝和出血时间作用,还具有抗氧化作用, 消除体内自由基[4], 抑制突变和抗肿瘤作用[5]。绿原酸及其衍生物在抗HIV的研究中表现出一定的抑制效果。对绿原酸生物活性的研究已经逐渐深入到食品、保健品、医药和日用化工等多个领域[2]。绿原酸因此被称为植物黄金。现在的纯品绿原酸的市场价格为每20mg为108.00元。 葵花籽含绿原酸1.0%~4.5%,平均为2.8%,从葵花籽中提取绿原酸具有实用价值, 同时还能避免由于绿原酸的存在引起葵花分离蛋白变黑的现象[1]。本文采用的原料是水酶法葵花籽提油后离心分离出的水浸提液,该液体中含有绿原酸、低聚糖、少量蛋白及果胶等,采用水提醇沉方法提取绿原酸。目前国内以水酶法提取葵花籽油脂后分离出的水浸提液为原料提取绿原酸的研究还未见其它报道。 1 材料与方法 I.I 原料与试剂 葵花籽: 市售: 浸提液:葵花籽水酶法提取油脂后的浸提液,呈深绿色,固形物含量在5%~6%之间,略显浑浊过滤后放置备用。 绿原酸标准品: 中国药品生物制品鉴定所产品。 1.2 仪器 旋转蒸发器:上海亚荣生化仪器厂;离心机:北京离心机厂。 1.3 方法 1.3.1 绿原酸含量的测定【 】 采用紫外分光光度法。精确称取绿原酸标准品5.5 mg,置于5Oml容量瓶中,摇匀配制成绿原酸标准液,取0,5、0.75、I.O0、I.25、2.O0、2.50m1分别置于10ml比色管中,稀释至刻度 用分光光度计在200~800nm波长范围内进行扫描。找到最大吸收波长329nm。在329nm处测吸光度OD,以绿原酸标品浓度为横坐标,以OD 为纵坐标绘图, 以30% 甲醇做参比,得到回归方程:A=42.763C+0.0259,R=0.998,其中C代表浓度㈣,A代表吸光度。将经真空冷冻干燥得浸提样品200.0mg,用30%的甲醇溶解至100ml,从中吸取1ml再定容到100ml,取样在329nm下测吸光度值,代入回归方程计算样品中绿原酸的含量。例如:测得吸光度为0.652,计算可得C=0.0156g/L,可计算出200.0mg粗品绿原酸中绿原酸的质量为156.0,因此,绿原酸的纯度为:156.0/200.0×100%=78%。 1.3.2 总糖的测量 采用葸酮比色法。 1.3-3 绿原酸的提取工艺流程 水酶法提油后分离出的水浸提液一过滤一真空浓缩到适合固形物浓度-.-an入95% 的乙醇一抽滤一滤液收集一再次加入95% 的乙醇一抽滤一收集滤液一合并两次滤液一真空浓缩一冷却收集析出的晶体。 2 结果与讨论 葵花籽中含绿原酸1.0%~1.5%,多糖12%左右。水酶法提油后分离出的水浸提液中主要含有绿原酸、多糖、少量蛋白、果胶等。提取绿原酸的最大障碍是多糖。绿原酸和多糖都易溶解于水,但绿原酸还易溶于乙醇,而多糖类物质难溶于乙醇,采用高浓度乙醇沉淀多糖,过滤可将多糖从溶液中除去,可得到纯度较高的绿原酸,同时也得到一定纯度的多糖。实验证明,用95%的乙醇溶液多次沉淀多糖比一次沉淀效果好。由于乙醇在加入浸泡液时被稀释,对多糖的沉淀不利,也加大乙醇的用量,从经济和效率双方面考虑, 在加入乙醇之前先对浸泡液进行真空浓缩,提高溶液中固形物含量。由于绿原酸有长时间受热容易分解的性质,浓缩过程中要求真空度较高。在提取绿原酸的流程中影响绿原酸提取率的主要因素是真空浓缩后溶液的浓度和每次加入酒精的量。 2.1 浸泡液真空浓缩终点浓度的确定 取浸泡液分装存烧杯中。真空浓缩到不同的终点浓度,提取绿原酸,称量绿原酸的质量并计算其纯度。实验结果如表1所示。
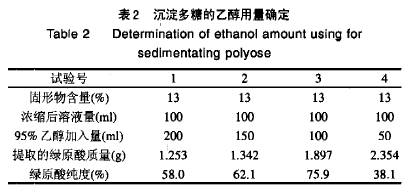
表1确定的四个浸泡液真空浓缩后浓度是根据多次实验得出的。离心前,固形物含量在5%~6% 之间,澄清。当浸泡液真空浓缩到固形物含量8% 左右时,浓缩液变混浊,离心分离后证明混浊物为蛋白质;离心后的清液继续浓缩,当固形物含量1 3% 时,溶液再次变混浊,离心后固体量非常少,测得此固体中含有绿原酸、蛋白和大分子多糖;此时离心后继续浓缩, 当固形物含量2 1% 左右时,液体明显变得粘稠,此时液体中含有的多糖开始析出, 当固形物含量31% 以上时,液体粘稠度很大,没有析出物。从纯度和绿原酸得率双面考虑, 当真空浓缩到固形物含量为13% 时加入乙醇为适宜。固形物含量越低,乙醇加入量越大,后步浓缩量也大,真空浓缩加热时间延长,会造成绿原酸的损失。当固形物含量1 3% 以上,随着多糖浓度的增加,部分多糖会包裹绿原酸,在加入乙醇后,在多糖沉降的同时包裹的绿原酸也随之沉降,造成绿原酸的损失。因此,选择浸泡液真空浓缩到固形物含量1 3%。 2.2 乙醇用量的确定 取浸泡液分装在烧杯中,确定乙醇的加入量。表2为实验结果。
期的浓缩量。从以 实验结果看出, 乙醇与浸泡液的体积比为1:1较适宜。 3 结论 水酶法提油后的浸泡液进行真空浓缩到固形物含量1 3% 时,加入此时溶液量1倍的95% 乙醇两次, 沉降多糖,然后继续真空浓缩,冷却可析出纯度为75.9%以上的绿原酸。 参考文献: 【1】 陈少洲.葵粕中绿原酸的研究进展与应用前景【J】l食品与发酵工业,2002,(3):5 1-52. 【2】 刘军海,等,绿原酸及其提取纯化和应用前景【J】.粮食与油脂,2003,(9):44. 【3】 李新兰.保健食品开发及应用[M】.武汉:华中理工大学出版社,2000. 【4】 Ohnishi M,et a1.Inhibitory efects of c~omgemc acids Of lihaleic acid peroxidation and haemdysis[J].Phytochemistry,1994,36(3):579-583. 【5】 陈迪华,等.天然多酚成分研究进展[M】.国外医药(植物药分册),1997,12(1):9-15. 【6】 陈乃炽,等,从杜仲叶中提取绿原酸纯品的研究【J】.西北林学院学报,1996,(11):58.60. 产品链接: 杜仲提取物 绿原酸 金银花提取物 苦杏仁苷 枇杷叶提取物-熊果酸 大花紫薇提取物-科罗索酸 上禾生物 专注植提 精于高纯 基于您对天然产物需求持续创新 |







 水提醇沉法从葵花籽中提取绿原酸
水提醇沉法从葵花籽中提取绿原酸