| 高效液相色谱法测定杜仲颗粒中京尼平苷酸和绿原酸的含量 |
| 发布时间:2010-12-03 信息来源:admin 发布人:admin 点击次数:3024 |
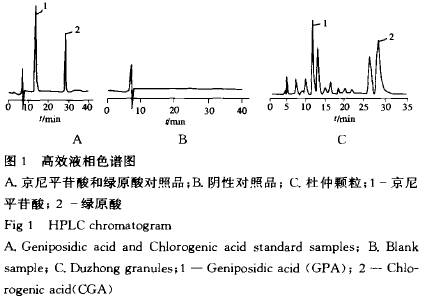
彭密军1,2 ,张敏1,刘建兰1,周春山2(1.吉首大学,湖南张家界427000;2.中南大学化学化工学院,湖南长沙410083) [摘要] 目的:建立杜仲颗粒中两种活性成分京尼平苷酸和绿原酸快速、同时测定的方法。方法:采用反相高效液相色谱法(RP-HPLC)测定,C18色谱柱(250mm×4.6mm,5 m),甲醇-水-冰乙酸(14.5:85:0.5)为流动相,流速1 mL・min-1 ,柱温25℃ ,检测波长236 nm,灵敏度:0.08 AUFS,进样体积6ul。结果:该方法线性关系良好,京尼平苷酸和绿原酸的回收率分别为99.03 ,99.99 ,测定结果RSD分别为0.134% ,1.72%。结论:该法快速、可靠、简单、灵敏度高。 [关键词] 高效液相色谱法;杜仲颗粒;京尼平苷酸;绿原酸 杜仲颗粒系中成药,主要含杜仲皮和杜仲叶提取GPA)和绿原酸(chlorogenic acid,CGA)。该制剂能够增强机体的免疫功能,对细胞免疫功能具有双向调节作用;并有利尿、镇静及抑制肠道对胆固醇吸收的作用;还可调节子宫收缩,对先兆流产有很好的疗效;具有缓和而持久的降压作用[1~3],并能与自由基结合抑制脂质过氧化反应,起到抗衰老作用[4~7]。本研究采用RP_HPLC法对杜仲颗粒中的两种主要活性成分GPA和CGA的含量进行同时测定,现报道如下。 1 材料 Biotronik液相色谱分析仪(德国BIoTRoNIK公司)。绿原酸对照品(中国药品生物制品检定所);京尼平苷酸标准样品(日本和光纯药业株式会社);杜仲颗粒(贵州天方药业有限公司生产,批号:020422,020426,020428);纯化水,乙醇,甲醇,冰醋酸为分析纯。试剂配制后应当用0.45 m微孑L滤膜过滤。 2 方法与结果 2.1 色谱条件及系统适应性试验 2.1.1 色谱条件色谱柱:Polygosil C 8色谱柱(250mm×4.6 mm,5 m);流动相:甲醇一水一冰乙酸(14.5:85:0.5);流速:1.0 mL・min-1,柱温:25℃ ,检测波长:236 nm;灵敏度:0.08 AUFS;进样体积6 ul。色谱图见图1。
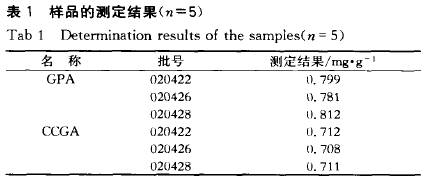
2.1.2 系统适用性色谱柱理论塔板数(N)按京尼平苷酸计酸为5200,与相邻峰分离度≥ 1.5,拖尾因子为1.15;按绿原酸计算N为5500,拖尾因子为1.08。 2.1.3 测定波长的选择分别取绿原酸和京尼平苷酸对照品溶液于紫外光区190~400 nm 范围内进行扫描,CGA的最大吸收波长在325 nm,第二吸收波长为238 nm,GPA的最大吸收波长则在235 nm左右,确定236 nm为测定波长。 2.2 对照品溶液的制备准确称取GPA对照品6.8mg、CGA对照品7.1 mg,用色谱纯甲醇溶解并定容至5 mL,得到浓度为1.36 g・L-1的GPA、1.42 g・L-1的CGA对照品混合储备液,冷藏保存。 2.3 样品溶液的制备 准确称取0.1 g杜仲颗粒样品,加人适量50 的甲醇一水溶液,超声溶解20 min 2次,移人25 mL量瓶中,再用50%的甲醇一水溶液定容至刻度,摇匀,过滤。准确吸取滤液1.0 mL于10mL量瓶中,用流动相稀释、定容至刻度,摇匀。用0.45um滤膜过滤后,即得待测液。 2.4 线性关系考察取对照品储备液用流动相溶液稀释,配制成对照品系列混合溶液,GPA:0.034,0.068,0.136,0.272,0.544 g ・I -1 ;CGA :0.034,0.071,0.142,0.284,0.568 g・L-1。各进样6ul,平行5次。结果GPA和CGA的峰面积y与其进样浓 度X(g・L-1)存在良好的线性关系: CGA :Y = 一608 71+ 4 322 500X ,r= 0.998 6,线性范围:0.036~0.568 g・L-1 GPA:Y = 一377 20+ 6 043 800X ,r= 0.996 9,线性范围:0.034~0.544 g・L-1 2.5 精密度试验精密吸取GPA含量为0.080 g・L-1;CGA为0.072 g・L-1 的样品溶液6 ul,重复进样5次,测得RSD分别为:GPA 0.61 %,CGA 0.72 %(n= 5)。 2.6 稳定性实验精密吸取GPA含量为0.080 g・L-1;CGA为0.072 g・L-1的混合溶液6 ul,每间隔一段时间进样测定一次,实验表明,该混合溶液在10 d内基本稳定。 2.7 加标回收率测定精密称取适量的已测定含量的样品5份,分别加人一定量的GPA、CGA对照品,采用2.3方法制备样品,过滤后分析,测定回收率,结果平均含量分别为99.03%,99.99%。 2.8 重复性试验 按“2.3”项制备杜仲颗粒样品溶液,进样6 ul,重复5次。试验结果测得GPA,CGA含量分别为0.799,0.712 mg・g-1,RSD 分别为0.134%,1.72%。 2.9 样品的测定分别对3批杜仲颗粒样品进行测定,各样品中GPA、CGA的含量测定结果见表1。
3 讨论 3.1 样品提取方法的选择取同一样品4份,分别加甲醇、乙醇、50%的甲醇及50%的乙醇同时超声波提取20 min提取,各两次,合并后测定其中GPA 和CGA含量。结果表明,50%的甲醇提取率最高,提取最完全,所以确定用50%的甲醇为提取溶剂。 3.2 测定方法的选择GPA及CGA的测定方法主要有分光光度法,薄层色谱法和高效液相色谱法等[3-8]。大多是对杜仲中的两种成分分别进行分析测定,而对杜仲制剂中的这两种化合物同时进行测定的方法未见有报道。高效液相色谱法能分离并检测各个有关组分,而且方法快速、准确。 3.3 流动相的选择 试验发现,仅以不同比例的甲醇一水为流动相,由于两种组分都有羧基,极性均很强,在C 18柱上都不易保留,很快被流动相洗脱下来,难以完全分离。流动相中加入醋酸,可抑制GPA 和CGA羧基的离解,延长其保留时间,从而使之与其他杂质分 离彻底。两色谱峰峰形都有所改善,所得色谱图峰形对称。甲醇一水一醋酸的比例为14.5:85:0.5时,所测定组分与附近分离较好,整个分析时间也较适宜(35 min可完成)。 参考文献: [1] 阴健.中药现代研究与临床应用[M].北京:学苑出版社,1993.339 [2] San,RHC,Chan RIM.Inhibitory effect of Phenolic compounds on Aflatoxin B1 Metabolism and Induced Mutagenesis[J].Mutation Res,1987,177:229. [3] Metori K .Tanimoto S,Takahashi S.Promotive effect of Eucom―mia leaf extract on collagen synthesis in rats[J].Nat Med,1998,52:465. [4] 赵晖.杜仲叶药理作用研究(II)抗衰老作用[J].国外医学中医中药分册,2000,22(3):151. [5] Nakamura T.Nakazawa Y,Onizuka S.et a1. Antimutagenicity of Tochu tea(an aqueous extract of Eucommia ulmoides leaves).Nakamura T.Nakazawa Y,Onizuka S.et a1. Antimutagenicity of Tochu tea(an aqueous extract of Eucommia ulmoides leaves). The clastogen―suppressing effects of Tuchu tea in(、H()ceils and mice[J].Mutation Research/Genetic Toxicology and Environ―mental M utagenesis,1 997,388:7. [6] I i Y.Sato T.Metori K.et a1.The promoting effects of genipo sidic acid and aucubin in Eucommia ulmoides()live leaves on colla―gen synthesis[J].Biol Pharm Bull,1998,21:1306. [7] Deyama T.Nishibe S,Nakazawa Y.Constituents and pharmaco logical effects of Eucommia and Siberian ginseng[J].Acta phar―macol Sin,2001,22(12):1057. [8]Kawasaki T,Uezono K,Nakazawa Y. Antihype rtensive mecha―nism of food for specified health use:Eucommia leaf glycoside and hs clinical apptication[J].J Heahh S,ci,2000,(22):29
产品链接: 杜仲提取物 绿原酸 金银花提取物 苦杏仁苷 枇杷叶提取物-熊果酸 大花紫薇提取物-科罗索酸 上禾生物 专注植提 精于高纯 基于您对天然产物需求持续创新 |







 高效液相色谱法测定杜仲颗粒中京尼平苷酸和绿原酸的含量
高效液相色谱法测定杜仲颗粒中京尼平苷酸和绿原酸的含量